催化剂的影响
实验探究
实验操作:

实验现象:加入
溶液的试管中产生气泡的速率更快。 实验结论:加入催化剂可以加快反应速率。
催化剂相关结论
- 催化剂是能改变化学反应速率但在反应前后本身的质量和化学性质都不变的物质。
- 有的催化剂能加快化学反应速率,叫正催化剂;有的催化剂能减慢化学反应速率,叫负催化剂。若无特殊说明,一般催化剂是指正催化剂。
- 催化剂具有选择性,即不同的化学反应一般需要不同的催化剂。
温度的影响
实验探究
实验操作:

实验现象:浸在热水中的试管内产生气泡的速率明显比浸在冷水中的试管产生气泡的速率快。
实验结论:其他条件相同时,升高温度可以加快化学反应速率。
温度影响结论
- 升高温度,化学反应速率加快;降低温度,化学反应速率减慢。
- 实验测得,其他条件相同时,温度每升高10℃,化学反应速率通常增大到原来的2-4倍。
- 温度对化学反应速率的影响对任何反应都适用,且与反应物的状态无关。
浓度的影响
实验探究
- 实验操作:
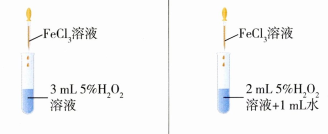
- 实验现象:不加水的试管产生气泡的速率更快。
- 实验结论:其他条件相同时,浓度越高,反应速率越快。
温度影响结论
其他条件相同时,增大反应物的浓度,可以增大化学反应速率;减小反应物的浓度,可以减小化学反应速率。
浓度对化学反应的影响只适用于在溶液中进行或有气体参加的反应。
固体、纯液体(如水)的浓度视为常数,对于这些反应物,改变他们的量不会引起浓度的变化,不影响化学反应速率。如:
改变
的量,化学反应速率不变。
压强的影响
对于有气体参加的反应,当其他条件不变时,增大压强可以增大反应速率。
改变压强本质是引起了浓度的改变。
增大压强相当于增大反应物的浓度,化学反应速率加快;减小压强相当于减小反应物的浓度,化学反应速率减慢。
若参加反应的物质为固体或液体(溶液),由于压强的变化对它们的浓度几乎无影响,可以认为反应速率不变。
充入惰性气体对反应速率的影响
稀有气体或其他不参加反应的气体充入反应容器,对反应速率的影响分为以下两种情况:
- 恒温、恒容:充入的稀有气体或其他不参加反应的气体虽增大了容器的总压强,但却没有改变反应气体的分压,即没有改变反应物的浓度,故不改变反应速率。
- 恒温、恒压:充入的气体会使反应容器容积扩大,虽未减小压强,但却减小了反应气体的分压,即降低了反应物的浓度,故使反应速率降低。
其他因素
- 光照可以增大某些反应的反应速率;
- 形成原电池也可以增大反应速率;
- 反应物颗粒的大小;
- 溶剂的种类;
- 超声波、放射线、电磁波等因素也能影响反应速率。
不同情况下化学反应速率大小的判断
相同条件下同一反应
看能否构成原电池,构成原电池的可增大化学反应速率。
定量比较:对于同一化学反应,将不同物质的反应速率转化成同一物质后,再比较大小。
或将不同物质表示的速率值,除以化学方程式中各物质的化学计量数,然后比较大小。比值大的反应速率大。
不同条件下同一反应:根据外部条件(浓度、温度、压强、催化剂)对化学反应速率影响的规律比较反应速率大小。
相同条件下不同反应:根据反应物本身的性质比较反应速率大小。
在相同条件下,不同反应中,反应物的化学性质越活泼,化学反应速率越大。